LINEE GUIDA PER LA GESTIONE DELLE PRODUZIONI MANGIMISTICHE NELLA FILIERA NON-OGM
Redatto da:

Ugo Marchesi, Annalisa Paternò, Daniela Verginelli, Centro di Referenza Nazionale per la ricerca di OGM
Istituto Zooprofilattico Sperimentale del Lazio e della Toscana


Angelo Millone, Viveca Righi -Dipartimento di prevenzione, ASL CN1 Cuneo

Carlo Brera, Marzia De Giacomo, Barbara De Santis, Roberta Onori,Reparto OGM e Xenobiotici di origine fungina – Istituto Superiore di Sanità
- Premessa
- Gli OGM nel settore alimentare e mangimistico
- Gestione della produzione dei mangimi non GM
- Procedure di attivazione della produzione di mangimi non-GM
- Sistema di autocontrollo per la produzione di mangimi non-GM
- Piano di campionamento e flusso analitico
- Allegato 1
- Allegato 2
- Allegato 3
Gli Organismi Geneticamente Modificati (OGM) sono definiti dalla legislazione europea come “organismi, il cui materiale genetico è stato modificato in modo diverso da quanto si verifica in natura mediante accoppiamento o incrocio o con la ricombinazione genetica naturale” (1Direttiva 2001/18/CE).
Gli elementi fondanti dell’attuale normativa europea in materia di OGM sono entrati in vigore nel 2004 (2Reg.(CE) 1829/2003, 3Reg (CE) 1830/2003) con il duplice obiettivo di:
• proteggere la salute umana ed animale nonché l’ambiente: un OGM può essere immesso sul mercato solo se autorizzato a seguito di un’accurata valutazione del rischio;
• assicurare la libera circolazione di beni all’interno dell’Unione Europea.
Nell’ultimo ventennio lo sviluppo di colture geneticamente modificate (GM) e la superficie deputata alla loro coltivazione sono aumentati considerevolmente. In particolare le piante GM più diffuse presentano tolleranza agli erbicidi, primo fra tutti il glifosato, in quanto questo risulta il metodo relativamente più economico ed efficace per il controllo in campo delle infestanti, ma molto utilizzate sono anche quelle recanti resistenze a parassiti e virus.
In relazione alla produzione agricola globale si evince che la soia geneticamente modificata ha avuto ed ha un’ampia distribuzione, interessando oggi la quasi totalità delle aree coltivate a soia. Non di minore importanza, anche se con percentuali più basse, sono le coltivazioni GM di mais, cotone e colza (4Clive James 2016).
1Direttiva 2001/18/CE del Parlamento europeo e del Consiglio del 12 marzo 2001 sull’emissione deliberata nell’ambiente di Organismi Geneticamente Modificati e che abroga la Direttiva 90/220/CEE del Consiglio. Gazzetta ufficiale delle Comunità europee n.106 del 17-4-2001.
2Regolamento (CE) n. 1829/2003 del Parlamento Europeo e del Consiglio del 22 settembre 2003 relativo agli alimenti e ai mangimi geneticamente modificati. Gazzetta Ufficiale dell’Unione europea n. 268 del 18-10-2003.
3Regolamento (CE) n. 1830/2003 del Parlamento Europeo e del Consiglio del 22 settembre 2003 concernente la tracciabilità e l’etchettatura di organismi geneticamente modificati e la tracciabilità di alimenti e mangimi ottenuti da organismi geneticamente modificati, nonché recante modifica della direttiva 2001/18 CE. Gazzetta ufficiale dell’Unione europea n.268 del 18-10-2003
4Clive James. Global status of commercialized biotech/GM crops: 2014. ISAAA brief 49-2014 https://www.isaaa.org/resources/publications/briefs/52/download/isaaa-brief-52-2016.pdf
Nel 2003 la necessità di armonizzare il quadro normativo a livello comunitario in entrambi i settori dell’alimentazione umana ed animale, nel rispetto del principio “dai campi alla tavola” sancito dal Libro Bianco sulla sicurezza alimentare, ha portato all’emanazione del Regolamento (CE) 1829/2003 e del Regolamento (CE) 1830/2003. Tali Regolamenti (vedi allegato 1) hanno definito
da un lato una procedura univoca ed armonizzata per l’autorizzazione di OGM ad impiego alimentare e mangimistico, dall’altra i requisiti di etichettatura e di tracciabilità degli alimenti e dei mangimi geneticamente modificati autorizzati all’interno dell’Unione Europea;
la Direttiva 2001/18/CE riguarda invece l’immissione deliberata di OGM nell’ambiente, recentemente modificata dalla 5Direttiva (UE) 2015/412, recepita con Decreto Legislativo 14 Novembre 2016 n.227, per quanto concerne la possibilità per gli Stati membri di limitare o vietare la coltivazione di organismi geneticamente modificati (OGM) sul proprio territorio. Tali modifiche sono intervenute nel tentativo di meglio regolamentare la coltivazione di OGM agroalimentari nell’UE, tradizionalmente piuttosto controversa ed articolata in virtù di norme nazionali adottate da diversi Stati Membri per impedirne di fatto la realizzazione.
Attualmente solo alcuni Paesi coltivano OGM: Spagna, Portogallo, Repubblica Ceca, Slovacchia , benché il totale di ettari di colture transgeniche (si tratta esclusivamente di mais) rappresenti una percentuale minima della superficie agricola utilizzata.
Al contempo, la già citata normativa comunitaria ha introdotto, nel mercato interno, la libera circolazione degli OGM “autorizzati” ed il loro impiego entro i limiti consentiti. In particolare, la normativa UE prevede che tutti gli OGM utilizzati nel settore alimentare (alimenti e mangimi), per poter essere immessi sul mercato europeo devono aver ultimato il processo di autorizzazione cosi come previsto dal Reg(CE) 1829/2003.
Inoltre, per le norme di tracciabilità,
tutti i prodotti che contengono o sono costituiti da OGM devono essere etichettati per la presenza di OGM > 0,9% rispetto al singolo ingrediente, mentre non sussiste obbligo di etichettatura a percentuali di OGM ≤ 0,9%, purché tale presenza sia accidentale o tecnicamente inevitabile
e gli operatori devono dimostrare di avere preso tutte le misure appropriate per evitarne la presenza. Questa tipologia di etichettatura è definita “Etichettatura positiva” in quanto segnala la presenza di OGM. Per contro etichettare alimenti/mangimi per evidenziare l’assenza di OGM, la cosiddetta “etichettatura negativa”, in prodotti che non contengono OGM non è ancora regolamentata a livello europeo.
La situazione nei diversi Stati Membri è pertanto estremamente variegata e a tal riguardo la Commissione Europea nel 20136 ha condotto uno studio sulla etichettatura “OGM-free” (intendendo con tale dicitura sia l’indicazione di un prodotto privo di OGM sia di un processo privo di OGM) con l’obiettivo ultimo di armonizzare tale dicitura nel contesto europeo.
Da questo studio è emerso come in alcuni Stati Membri siano presenti linee guida e in alcuni casi anche un supporto legislativo per facilitare l’utilizzo di etichettatura che attesti l’assenza di OGM (ad esempio in Germania in Austria in Francia e in Olanda), mentre in altri paesi (quali la Svezia) la legislazione addirittura vieta questo tipo di etichettatura.
In Italia il non uso di OGM (non-OGM) fa spesso parte del pacchetto di requisiti previsti da specifici disciplinari di produzione (ad es. biologico, DOP, IGP)
il che rende generalmente superflua e ridondante una ulteriore etichettatura negativa del prodotto non-OGM.
Ciononostante, sia in ambito mangimistico che nell’alimentazione umana, diversi operatori, per motivi di marketing, preferiscono rendere esplicita indicazione al consumatore. Tale interesse è dimostrato dall’esistenza di una attività di certificazione non-OGM, i cui requisiti minimi sono codificati da un 7Regolamento Tecnico di ACCREDIA (Ente Italiano di Accreditamento)
La produzione non-OGM abbraccia il settore biologico, che è disciplinato secondo il 8Reg (EC) 834/2007 (relativo alla produzione biologica e all’etichettatura dei prodotti biologici) ma parallelamente a questa regolamentazione si è assistito anche alla diffusione di prodotti non-OGM da parte di alcune aziende sulla base di specifiche richieste del cliente (ad esempio disciplinari di produzione, o particolari politiche commerciali della catena di distribuzione).
Per quelle materie prime per cui la produzione nazionale non è sufficiente a soddisfare il mercato non-OGM, l’approvvigionamento deve necessariamente avvenire all’estero. Ciò avviene principalmente per la soia, che rappresenta la principale fonte proteica della stragrande maggioranza dei mangimi ad uso zootecnico. Essendo la soia la materia prima più “critica”, la sua gestione rappresenta l’obiettivo prioritario cui i produttori di mangimi non-OGM pongono particolare attenzione.
Le aziende mangimistiche devono operare una accurata selezione dei fornitori più affidabili, in grado di consegnare merce non solo certificata ma effettivamente priva di contaminazioni transgeniche.
Tuttavia l’intero impianto deve essere accuratamente controllato e gestito in quanto le contaminazioni crociate possono avvenire in qualsiasi punto della catena produttiva. Questo ha contribuito a comprendere l’esigenza di revisionare radicalmente la gestione delle produzioni, a partire dal trasporto e dallo stoccaggio delle materie prime fino al confezionamento, allo stoccaggio e trasporto dei prodotti finiti.
Ogni stabilimento di produzione ha quindi affrontato il problema della separazione delle linee produttive convenzionali e non-OGM in funzione delle proprie caratteristiche impiantistiche e gestionali. Alcuni hanno dedicato l’intero impianto a produzioni non-OGM, oppure sdoppiato le linee produttive, altri hanno delegato a terzi alcune loro produzioni, mentre altri ancora, viste le difficoltà, hanno rinunciato a questa fetta di mercato.
Occorre precisare che oggi i mangimi prodotti a partire da materie prime prive di OGM vengono principalmente utilizzati per due categorie di animali da reddito, bovini da carne e galline ovaiole inseriti in filiere qualificate attraverso l’applicazione di disciplinari di produzione che ne garantiscono le specifiche caratteristiche.
Uno strumento importante che supporta le scelte gestionali del processo produttivo è la verifica analitica. L’evoluzione e l’armonizzazione delle procedure analitiche e di campionamento hanno permesso di superare le iniziali difficoltà. Inoltre la corretta applicazione del 9Reg. CE 183/2005, che stabilisce i requisiti per l’igiene dei mangimi, con l’obiettivo di garantire la sicurezza dei mangimi lungo l’intera filiera alimentare, ha esteso la responsabilità delle produzioni degli alimenti zootecnici a tutti gli attori della filiera e ha contribuito anche a determinare una crescita culturale di tutte le componenti, ognuna per le proprie competenze.
Ciò nonostante, attualmente in materia di OGM non esistono ancora delle indicazioni chiare per stabilire procedure di autocontrollo che supportino le produzioni non-OGM.
Questo documento ha lo scopo di fornire strumenti utili al produttore di mangimi non-OGM per l’implementazione del proprio piano di autocontrollo, con particolare riferimento alle diverse tipologie d’impianto.
5DIRETTIVA (UE) 2015/412 DEL PARLAMENTO EUROPEO E DEL CONSIGLIO dell’11 marzo 2015 che modifica la direttiva 2001/18/CE per quanto concerne la possibilità per gli Stati membri di limitare o vietare la coltivazione di organismi geneticamente modificati (OGM) sul loro territorio. Gazzetta ufficiale dell’Unione europea n.068 del 13-3-2015
6DG SANCO, European Commission, final report State of play in the EU on GM-free food labelling schemes and assessment of the need for possible harmonisation. ISBN 978-92-79-49485-7 doi: 10.2875/4437. (http://www.europa.eu)
7RT 11 – 01/02/2017 – Requisiti minimi per la certificazione di prodotti con caratteristica/requisito NON OGM- Rev 00
8Regolamento (ce) n. 834/2007 del Consiglio del 28 giugno 2007 relativo alla produzione biologica e all’etichettatura dei prodotti biologici e che abroga il regolamento (CEE) n. 2092/91. Gazzetta ufficiale dell’Unione europea n. 189 del 20-7-2007
9REGOLAMENTO (CE) N. 183/2005 DEL PARLAMENTO EUROPEO E DEL CONSIGLIO del 12 gennaio 2005 che stabilisce requisiti per l’igiene dei mangimi. Gazzetta Ufficiale dell’Unione europea dell’8-2-2005
Il principio della coesistenza è stato introdotto nell’Unione Europea con lo scopo di consentire la libera scelta dei coltivatori e dei produttori di utilizzare i sistemi di coltivazione e produzione che ritengono più idonei, comprese le colture GM autorizzate in Europa. Questa scelta prevede la realizzazione di misure atte a prevenire eventuali cross-contaminazioni (contaminazioni crociate) lungo tutta la filiera produttiva.
In un stabilimento mangimistico le produzioni non-GM possono avvenire in:
- uno stabilimento dedicato (scelta migliore per evitare le 10contaminazioni crociate e da 11carry over);
- su una linea di produzione dedicata ai mangimi non-GM;
- sulla stessa linea di produzione dei mangimi convenzionali, adottando i dovuti accorgimenti.
Tabella 1. Punti di forza e debolezza delle diverse strategie di produzione mangimi non-GM
| MODALITA’ DI PRODUZIONE | PREREQUISITI | PUNTI DI FORZA | PUNTI DEBOLI |
| 1) Stabilimento dedicato alla produzione di mangimi non-GM |
|
|
|
| 2) Segregazione spaziale: linea di produzione dedicata |
|
|
|
| 3) Segregazione temporale: lavaggio della linea di produzione prima dell’inizio della produzione non-GM |
|
|
|
Una panoramica sui punti di debolezza e di forza delle diverse strategie è mostrata nella tabella 1. Il terzo caso, in cui la linea di produzione è la stessa sia per prodotti GM che non-GM, è la strategia preferibile per piccole aziende dove gli spazi sono ridotti e anche la possibilità di stoccaggio risulta limitata. Per aziende più grandi con diversi siti di produzione è possibile dedicare un sito o linea di produzione esclusivamente per mangimi non-GM.
La linea di produzione unica (tipologia 3) è quella con il maggior rischio di contaminazioni da carry over, occorre quindi una accurata pianificazione e pulizia dell’impianto per garantire un’efficiente segregazione di filiera. La separazione temporale dei mangimi non-GM dalla produzione dei mangimi convenzionali (es. una giornata dedicata alla produzione di mangimi non-GM, orari/giorni/settimane diverse ecc) e un’accurata pulizia della linea di produzione con prodotti non-GM (es. tritello, cruscami), che saranno successivamente declassati a prodotti convenzionali, possono ridurre il rischio di contaminazioni. E’ inoltre necessario conoscere, validando analiticamente una procedura, la quantità di materiale che deve essere utilizzato per il lavaggio della linea di produzione, nonché il tempo adeguato da dedicare alla pulizia dell’impianto.
10Contaminazioni crociate: contaminazione di un mangime non GM con materiale GM, dovuta a contatto accidentale nella stessa fase di lavorazione
11Contaminazione da carry over: contaminazione di un mangime non GM con materiale GM, proveniente da fasi di lavorazione precedenti
E’ necessario, prima di iniziare la produzione di mangimi non-GM, informare il Servizio Veterinario dell’ASL competente, in modo tale da permettere agli organi di controllo di effettuare un’ispezione per accertare la conformità della gestione della nuova produzione mangimi non-GM. Non è prevista un’autorizzazione specifica ma l’autorità competente deve essere informata per poter disporre successivamente i controlli previsti.
Gli stabilimenti di produzione mangimi che decidano di produrre mangimi non-GM generalmente richiedono la certificazione da parte di enti certificatori, ma tale qualifica non è obbligatoria per procedere alla produzione di alimenti zootecnici non-GM.
Occorre stabilire le tipologie di mangime non-GM che si intendono produrre (completo o complementare), le specie di destinazione, le materie prime non-GM utilizzate (soia, mais, colza ecc), e soprattutto accertarne la provenienza.
Attualmente le richieste provengono principalmente dal settore bovino (carne e latte) ed avicolo (galline ovaiole).
Oltre alla tipologia di mangime occorre definire la dimensione del mercato da servire per i mangimi non-GM (locale, regionale, nazionale, comunitario/paesi terzi), e di conseguenza anche la quantità annua di mangimi non-GM da produrre, tenendo conto anche della quota parte riservata ai mangimi convenzionali per i quali è prevista anche la presenza di OGM autorizzati.
Prima di iniziare la produzione di una linea di mangimi non-GM è necessario prendere in considerazione alcuni aspetti fondamentali:
- caratteristiche dell’impianto
- approvvigionamento delle materie prime
- stoccaggio delle materie prime e dei mangimi finiti
- trasporto dei prodotti finiti
Il manuale di autocontrollo aziendale è lo strumento fondamentale per la gestione delle produzioni. La parte riguardante la produzione di mangimi non-GM deve essere integrata al manuale esistente oppure aggiornata (qualora già esistente) strutturandola prevedendo analisi e validazione di ogni singola fase:
PREREQUISITI – i prerequisiti sono le procedure, quali le GMP (Good manufacturing practices: buone pratiche di produzione), le SOP (Standard Operative Procedures: procedure operative standard), le GHP (Good Hygiene Practices: buone pratiche igieniche), che forniscono le basi per l’allestimento del piano HACCP. Devono essere presenti ed operative prima di iniziare le produzioni. I prerequisiti da integrare nel piano di autocontrollo aziendale sono quelli che riguardano la produzione di mangimi non OGM. I prerequisiti quali il controllo degli infestanti, la pulizia dell’impianto, il rifornimento idrico, la gestione dei rifiuti, la pulizia e manutenzione delle apparecchiature/utensili concernono tutto l’impianto e non solo la parte inerente alla produzione di mangimi OGM e possono rimanere invariati, seguendo l’aggiornamento periodico normale. Il sistema HACCP è un sistema che garantisce l’applicazione uniforme di gestione della sicurezza alimentare (Reg. (CE) 178/2002; Reg. (CE) 183/2005). Non è sempre necessario identificare CCP (punti critici di controllo). In alcuni casi sono sufficienti le GMP, GHP ed i prerequisiti per garantire la sicurezza alimentare (spesso tutti i pericoli possono essere controllati in modo efficace applicando corrette procedure e prerequisiti). I prerequisiti devono essere documentati, monitorati cosi come le eventuali azioni correttive.
In linea generale, un piano HACCP prevede di:
- elencare le materie prime impiegate ed i prodotti finiti;
- predisporre un diagramma di flusso con la descrizione di ogni fase;
- effettuare un’analisi dei pericoli;
- elencare i pericoli ed individuare gli eventuali CCP (es. utilizzo dell’albero delle decisioni);
- stabilire i limiti critici per ogni CCP;
- stabilire un sistema di monitoraggio per ogni CCP;
- stabilire le azioni correttive qualora il CCP non sia più controllato;
- procedura di verifica del corretto funzionamento sistema HACCP;
- predisporre una documentazione adeguata
La problematica OGM può essere affrontata in modo del tutto sovrapponibile alla gestione delle altre potenziali contaminazioni, crociate o da carry over (micotossine, antibiotici e chemioterapici, coccidiostatici, metalli pesanti ecc.), ossia controllare e validare ogni fase del processo. La figura1 mostra l’impianto di essiccazione di un sistema di produzione mangimistica.
Per quanto concerne la produzione di mangimi non-GM, in base alla tipologia di produzione scelta:
- stabilimento dedicato
- linea di produzione dedicata (segregazione spaziale)
- linea di produzione ad uso misto GM/non-GM (segregazione temporale)
Vengono di seguito riportati i punti chiave (riepilogati in tab. 2) e le strategie da seguire.
Stabilimento: costruzione, layout (2 e 3)
La planimetria dello stabilimento deve essere predisposta/integrata indicando:
- il percorso di mangimi non-OGM (scarico materie prime, stoccaggio, pesatura, macinazione, miscelazione, stoccaggio e carico prodotti finiti);
- le fosse di scarico materie prime, dedicate e non;
- gli impianti di aspirazione polveri nell’area scarico materie prime N.B. anche le polveri possono contaminare, non riutilizzare nei mangimi non-OGM;
- i silos dedicati per le materie prime e prodotti finiti non-OGM (numerazione univoca dei silos, sia sulla planimetria sia sui silos dello stabilimento);
- i silos dedicati per i prodotti per la pulizia della linea/linee produzione;
- le aree di stoccaggio materie prime/prodotti finiti non-GM in sacchi.
Materie prime: Qualifica dei fornitori (1, 2 e 3)
devono essere predisposti:
-
un elenco delle materie prime non-GM in arrivo;
- un elenco dei fornitori di materie prime non-GM (registrati/riconosciuti ai sensi del Reg. (CE) n. 183/2005) che devono essere referenziati e garantire che la materia prima in arrivo sia priva di OGM (al di sotto di un valore soglia adeguatamente basso, preferibilmente non al di sopra dello 0,2%). Le garanzie sono fornite mediante certificazioni attestanti l’assenza di materiale GM (al di sotto del valore soglia) e/o esiti analitici comprovanti la conformità delle materie prime per ogni fornitura o lotto;
- Le certificazioni di qualità più utilizzate per le materie prime non-GM sono le seguenti:
- Dichiarazione non-GM “once only”;
- Dichiarazione del lotto non-GM + esiti analitici;
- Certificato di approvvigionamento non-GM;
- Sistema di identità (identity preserved program) per singolo lotto e/o ingrediente.
Nel piano analitico aziendale devono essere previsti campioni per verificare la veridicità delle certificazioni. I test di validazione possono seguire diverse procedure confacenti alle diverse specifiche produttive.
Devono essere presenti inoltre:
-
-
-
- tutti i contratti stipulati con i fornitori di materie prime non-GM;
- una procedura che illustri il sistema di ricezione e stoccaggio delle materie prime non-GM ai fini della tracciabilità interna.
-
-
In alcuni casi non è sempre possibile ottenere certificazioni di alcune materie prime (es. mais, girasole) ed è quindi importante comprare tali materie prime da fornitori accuratamente referenziati e controllati mediante analisi effettuate periodicamente, nonché assicurarsi che i fornitori effettuino un trasporto dedicato.

Figura 1. Impianto di essiccazione
Gestione materie prime in arrivo: (2 e 3)
La gestione delle materie prime dipende dalla disponibilità o meno di fosse di scarico dedicate per le materie prime sfuse non-GM (in base al quantitativo del prodotto) e di silos di stoccaggio adibiti unicamente ai prodotti non-GM (allo svuotamento tutti i silos, dedicati e non, devono essere puliti a fondo). Non è sempre possibile avere fosse di scarico dedicate ed in tale caso è necessario predisporre una procedura di pulizia adeguata tra lo scarico di mangimi convenzionali e non-GM. E’ necessario predisporre un sistema di aspirazione delle polveri nell’area scarico materie prime – da non utilizzare nella filiera non-GM. I silos devono essere identificati ed indicati sulla planimetria dello stabilimento. Ogni lotto di materie prime non-GM in arrivo, provvisto di certificazione e possibilmente esito analitico accompagnato dalla bolla di consegna, deve essere identificato e registrato per garantire la tracciabilità lungo tutto il percorso della catena di produzione.
Pulizia degli impianti/attrezzature: (3)
E’ necessaria una procedura per la pulizia degli impianti/attrezzature utilizzate per la produzione mangimi non-GM che tenga conto di tutto il processo dalla fossa di scarico dedicata, ai silos materie prime e prodotti finiti dedicati, all’area di stoccaggio materie prime e prodotti finiti in sacchi.
Prevenzione delle contaminazioni: (2 e 3)
- Contaminazioni da carry over (3)
- Pulizia della linea di produzione e gestione dei prodotti “scopa” utilizzati;
- Indicazione dei prodotti di lavaggio utilizzati per la pulizia della linea di produzione es. tritello, cruschello ecc.;
- Pulizia dei filtri di aspirazione della fossa scarico;
- Identificazione silos di stoccaggio dei prodotti di pulizia ed indicazione della successiva utilizzazione del prodotto eventualmente contaminato con prodotti GM (declassamento nei mangimi “convenzionali”);
- Quantità del prodotto utilizzato oppure tempo di passaggio nella linea necessario per assicurare l’assenza di contaminazioni crociate, eventuale carry-over del mangime convenzionale prodotto in precedenza – il sistema deve essere validato;
- Successiva gestione ed utilizzo dei prodotti di lavaggio.
- Pulizia della linea: dopo lo scarico delle materie prime, dopo il dosaggio e la macinazione e dopo il carico dei prodotti finiti.
- Per le difficoltà di pulizia della pellettatrice (figura 2) si sconsiglia fortemente l’impiego di una linea di produzione ad uso misto GM/non-GM (tipologia 3 con segregazione temporale) per la produzione di mangimi pellettati non-GM

Figura 2. Pellettatrice
- Contaminazioni crociate (2 e 3)
- Pulizia della linea di produzione e gestione dei prodotti “scopa” utilizzati;
- Utilizzo di prodotti di lavaggio altamente abrasivi per la pulizia della linea di produzione es. farina di mais, crusca di frumento o farina d’orzo;
- Pulizia dei filtri di aspirazione della fossa di scarico e declassamento della prima merce successivamente introdotta;
- Identificazione dei silos di stoccaggio dei prodotti di pulizia e allestimento di griglia di produzione per le successive utilizzazioni del prodotto eventualmente contaminato con prodotti GM (declassamento nei mangimi “convenzionali”);
- Quantità del prodotto da utilizzare nella linea sufficiente per assicurare l’assenza di contaminazioni crociate dovute al mangime convenzionale prodotto in precedenza – il sistema deve essere validato con almeno tre prove corredate da analisi di laboratorio;
- Successiva gestione ed utilizzo dei prodotti di lavaggio controllata da software;
- Duplice pulizia della linea: dopo lo scarico delle materie prime, dopo il dosaggio e la macinazione e dopo il carico dei prodotti finiti;
- Evitare l’impiego di una linea di produzione ad uso misto GM/non-GM (tipologia 3 con segregazione temporale) per la produzione di mangimi pellettati non-GM
- Controllo sistematico di tutte le apparecchiature per prevenire fuoriuscite involontarie di mangime (paratie, snodi, coclee ecc.)
Tracciabilità e Rintracciabilità: (1, 2, 3)
-
- Predisporre un elenco materie prime non-GM (es. mais non-GM, farina di estrazione di soia non-GM), un elenco fornitori materie prime non-GM, un elenco prodotti finiti, un elenco clienti, la registrazione materie prime in arrivo-assegnazione n° per la tracciabilità in base alle bolle di consegna, un sistema di registrazione e archiviazione delle informazioni relative agli arrivi materie prime e lo stoccaggio in silos identificati, un sistema di registrazione ed archiviazione delle informazioni relative alle produzioni giornaliere con assegnazione del numero di lotto di produzione, l’identificazione del lotto prodotti finiti e tracciabilità
- Gestione non-conformità: l’autorità competente deve essere informata nel caso di riscontro di eventi GM in autocontrollo;
- Gestione richiamo-ritiro: i prodotti non conformi possono essere declassati a mangimi “convenzionali”. L’autorità competente deve essere informata;
- Disporre di silos per i prodotti non conformi
Formazione: (1, 2, 3)
Il piano di formazione (inerente alla produzione di mangimi non-GM) deve comprendere:
- l’elenco del personale e metodologia adottata per la formazione;
- trascrizione delle diverse attività formative con gli argomenti ed i relatori;
- la frequenza delle attività di formazione;
- l’obiettivo dei corsi di formazione;
- l’elenco dei partecipanti e valutazioni finali.
Stoccaggio materie prime e prodotti finiti (in sacchi): (2, 3)
All’interno dello stabilimento deve essere individuata ed identificata un’area separata (controllo spaziale) per lo stoccaggio delle materie prime/prodotti finiti non-GM in sacchi. E’ anche possibile avvalersi di silos dedicati, a patto che vengano mantenuti sotto stretto controllo funzionale in fase di alimentazione e di prelievo.
Sistema di trasporto: (1, 2, 3)
- Indicare se il trasporto viene effettuato dalla ditta o tramite conto terzi oppure entrambi;
- Assicurarsi che il trasporto conto terzi sia autorizzato ai sensi del Reg. (CE)183/2005, (in quanto l’autorizzazione ai sensi del 183/2005 per il trasporto conto proprio è compreso nell’autorizzazione dello stabilimento);
- Specificare se il trasporto materie prime e prodotti finiti sfusi è effettuato su mezzi dedicati (solo trasporto prodotti non-GM) oppure no;
- Descrivere il sistema di pulizia in caso di trasporto non dedicato dimostrandone la validazione (prodotto utilizzato, quantitativo, prima di ogni carico ecc.). I mezzi devono essere completamente svuotati, soffiati e puliti con prodotti di lavaggio (es. tritello);
- Dichiarazione pulizia mezzi trasporto.
Piano Analitico: (1, 2, 3)
Il piano analitico, che prevede il campionamento e la sua successiva analisi, è indispensabile per la verifica della conformità dei prodotti alle specifiche annunciate. Prevede punti e frequenza di controllo nelle fasi di:
- Validazione del sistema
- Mantenimento sotto controllo del sistema
Tabella 2. Gestione dei punti chiave in base alla tipologia d’impianto
| TIPOLOGIA 1
stabilimento dedicato NON-OGM |
TIPOLOGIA 2
linea di produzione dedicata NON-OGM (segregazione spaziale) |
TIPOLOGIA 3
linea di produzione ad uso misto GM/NON-GM (segregazione temporale) |
|
|---|---|---|---|
|
Stabilimento: costruzione, layout |
* |
* |
|
|
Materie prime: Qualifica dei fornitori |
* |
* |
* |
|
Gestione materie prime in arrivo |
* |
* |
|
|
Pulizia degli impianti/attrezzature |
* |
||
|
Prevenzione delle contaminazioni da carry over |
* |
||
|
Prevenzione delle contaminazioni crociate |
* |
* |
|
|
Tracciabilità e Rintracciabilità |
* |
* |
* |
|
Formazione |
* |
* |
* |
|
Stoccaggio materie prime e prodotti finiti (in sacchi) |
* |
* |
|
|
Sistema di trasporto |
* |
* |
* |
|
Piano Analitico |
* |
* |
* |
Per quanto riguarda le procedure di campionamento occorre fare riferimento alle “buone pratiche di campionamento” per garantire i requisiti minimi di qualità in applicazione della normativa di riferimento relativa al campionamento (vedi allegato 2).
I requisiti fondamentali di un buon campionamento devono garantire:
- la rappresentatività (numero di campioni elementari, numero di punti di prelievo, grandezza del campione globale e del campione finale);
- l’accurata omogeneizzazione del campione globale;
- la corretta conservazione del campione prima dell’analisi, in luogo fresco e asciutto, per evitare modificazioni fisiche della matrice ed alterazioni delle sostanze da ricercare;
- limitata esposizione alla luce;
- l’assenza di contaminazione dei campioni prelevati.
I campionamenti in autocontrollo dovrebbero rispettare i requisiti previsti per il controllo ufficiale (Allegato 8 Piano Nazionale di Controllo Ufficiale sull’Alimentazione degli Animali-PNAA. È necessario inoltre stabilire i CCP dove e con quale frequenza effettuare il campionamento e la successiva analisi.
Per predisporre un corretto piano analitico di ricerca degli OGM (vedi allegato 3) è necessario assicurarsi che il laboratorio di analisi sia accreditato per gli esami richiesti, in quanto esistono laboratori che eseguono analisi con metodi non accreditati fornendo risultati non sempre attendibili e sovrapponibili con gli esiti dei controlli ufficiali eseguiti dalle Autorità Competenti.
Per una descrizione del flusso analitico per la ricerca di OGM in un laboratorio del controllo ufficiale si rimanda all’allegato specifico (Allegato 3) considerando tuttavia che la strategia analitica ed il ventaglio di prove necessarie per l’autocontrollo potranno essere ritagliati in base ai fattori di rischio specifici per il tipo di prodotto e per l’impianto di produzione. Ciò al fine di ridurre i costi del piano analitico ed assicurarne la necessaria sostenibilità economica.
Il piano di controllo dovrà comprendere campionamenti ed analisi:
- sulle materie prime in entrata per verificare la qualifica dei fornitori. I controlli sulle materie prime dovranno accertare la veridicità delle garanzie fornite dalle ditte fornitrici in sede di stesura del contratto. Fondamentali sono anche i controlli sulle materie prime non target (convenzionali) es. girasole, frumento ecc. per la verifica di possibili impurezze botaniche GM;
- sui prodotti finiti per verificare l’assenza di materiale GM autorizzato (<0,9%);
- lungo l’impianto per verificare l’efficacia del sistema di produzione (pulizia dell’impianto, tempi di lavorazione ecc.) es. all’uscita del miscelatore per verificare e calcolare il carry-over di eventuali tracce di OGM provenienti dalle precedenti produzioni di mangimi convenzionali. (sistema di produzione 3)
Il punto di prelievo, la metodologia di campionamento ed il numero di analisi da effettuare devono essere stabiliti in base ad una valutazione del rischio del sistema di produzione.
Il numero di controlli potrà essere diminuito in base alla valutazione dei risultati dei controlli nel tempo, se, in un certo lasso di tempo, i campioni risultino sempre conformi (validazione di fornitori e processi).
Nella figura 3 è rappresentato in modo schematico un impianto di produzione di mangimi e sono evidenziati i punti di controllo dove effettuare il campionamento.
Per la valutazione dell’idoneità delle materie prime il prelievo può essere effettuato nel punto P1. Si può campionare in modo statico direttamente sul camion in arrivo, mediante l’uso di opportune sonde (sia in modalità manuale che in automatico mediante auto campionatori) o dinamico durante lo scarico. Anche in questo caso il prelievo può essere effettuato in modalità manuale mediante prelevi con un sessola ad intervalli di tempo regolari, o in automatico mediante auto campionatori posizionati lungo la linea di trasporto dalla fossa di scarico al silo.
I punti di controllo (Tab. 3) variano in base alla tipologia di produzione scelta: 1) stabilimento dedicato; 2) linea di produzione dedicata (segregazione spaziale); 3) linea di produzione ad uso misto GM – non GM (segregazione temporale).
- Per la valutazione dell’idoneità delle materie e quindi per la valutazione della conformità del fornitore, i punti controllo sono da individuare durante la fase di scarico (P1) (sistemi di produzione 1, 2 e 3) o lungo la linea di trasporto dalla fossa di scarico al silo di stoccaggio (P2). Nel secondo caso i valori riscontrati possono essere alterati da una eventuale contaminazione a livello di fossa di scarico e sistema di trasporto al silos. (sistemi di produzione 2 e 3).
- Per la valutazione della corretta separazione spaziale o temporale, il punto di controllo (P3), punto di carico della farina in bilancia permette di verificare l’assenza di contaminazione del silos di stoccaggio e della linea di trasporto alla bilancia ed il punto di controllo (P4) per la verifica relativa all’impianto di miscelamento e di produzione del prodotto finito (sistemi di produzione 2 e 3).
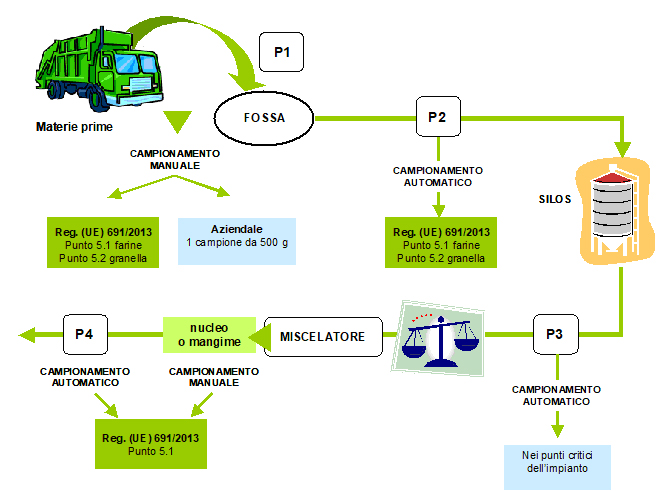
Figura 3. Rappresentazione schematica di un tipico impianto di produzione di mangimi
Tabella 3. Punti di controllo in base alla tipologia d’impianto
| TIPOLOGIA 1
stabilimento dedicato NON-OGM |
TIPOLOGIA 2
linea di produzione dedicata NON-OGM (segregazione spaziale) |
TIPOLOGIA 3
linea di produzione ad uso misto GM/NON-GM (segregazione temporale) |
|
|---|---|---|---|
|
Fase di scarico della materia prima(P1) |
* |
* |
* |
|
Lungo la linea di trasporto dalla fossa di scarico al silo di stoccaggio (P2) |
** |
* |
|
|
Punto di carico della farina in bilancia (P3) |
* |
||
|
Fase di produzione del prodotto finito (P4) |
* |
** Se si utilizza la stessa fossa di scarico per le due linee di produzione.
Nell’ambito del controllo ufficiale la metodologia di campionamento deve essere effettuata in base al Regolamento UE 691/2013 e all’allegato 8 del Piano Nazionale Alimentazione Animale (PNAA). Nel caso di autocontrollo la scelta della metodologia di campionamento da utilizzare può essere differente, va comunque sottolineato che procedure di campionamento meno rigorose comportano un aumento dell’errore legato al campionamento e quindi un aumento del rischio di avere una valutazione non corretta del contenuto “reale” di OGM nella porzione.
Frequenza dei controlli
La frequenza dei controlli va stabilita caso per caso in base a fattori di rischio legati alla fornitura ed alle caratteristiche strutturali e funzionali dell’impianto, sempre distinguendo le due fasi:
- Validazione del sistema Fase iniziale, di verifica, dove i controlli sono sistematici, o comunque frequenti, per raccogliere elementi conoscitivi utili a stabilire la frequenza dei controlli del sistema a regime;
- Mantenimento sotto controllo del sistema. Fase caratterizzata da controlli periodici, almeno semestrali, su processi già a regime.
Ad esempio, il controllo di un fornitore di granella di soia che si approvvigiona da paesi terzi, massimo profilo di rischio per la presenza di materiale GM, andrebbe configurato come segue:
- Validazione: campionamento rappresentativo e controllo analitico almeno dei primi tre lotti per verificare l’assenza di materiale GM;
- Mantenimento: campionamento rappresentativo e controllo analitico almeno semestrale della fornitura a regime
Per contro, forniture con profili di rischio inferiore, quali ad esempio materie prime con specie vegetali a basso rischio di contaminazione da OGM, o di produzione nazionale, potranno essere trattate come segue:
- Validazione: campionamento rappresentativo e controllo analitico del primo lotto per verificare l’assenza di materiale GM;
- Mantenimento: campionamento rappresentativo e controllo analitico semestrale della fornitura a regime.
APPROFONDIMENTI SULLE NORME PRINCIPALI
relative ad alimenti e mangimi GM
Regolamento (CE) n. 1829/2003 del Parlamento europeo e del Consiglio, del 22 settembre 2003, relativo agli alimenti e ai mangimi geneticamente modificati.Il regolamento 1829/2003 (in applicazione dal 18 aprile 2004) riguarda l’immissione sul mercato degli alimenti e mangimi geneticamente modificati e gli obiettivi ed aspetti principali di tale norma sono quelli di garantire un elevato livello di tutela della salute umana, animale e dell’ambiente, istituire una procedura comunitaria per l’autorizzazione e vigilanza degli alimenti e mangimi GM, nonché di stabilire norme per l’etichettatura di mangimi e alimenti geneticamente modificati.
- AutorizzazioneAl fine di proteggere la salute umana ed animale, gli alimenti ed i mangimi che contengono o sono costituiti da OGM o sono prodotti a partire da tali organismi, devono essere sottoposti a una procedura di autorizzazione. Tali disposizioni si applicano anche ai mangimi destinati agli animali non utilizzati per la produzione alimentare (animali non DPA – petfood);- L’immissione in commercio di un OGM destinato all’alimentazione umana e animale è possibile solo previa autorizzazione che si consegue al termine di un procedimento complesso, dove l’Autorità Europea per la sicurezza alimentare (EFSA European Food Safety Authority) svolge un ruolo cardine per la valutazione del rischio. L’EFSA è chiamata infatti ad esprimere un parere scientifico entro sei mesi dalla presentazione della domanda di autorizzazione da parte del notificante.- L’autorizzazione ha validità 10 anni
- Soglia di tolleranza di etichettaturaIl regolamento introduce una soglia di tolleranza di etichettatura e specifica che sono esentati dall’obbligo dell’etichettatura i mangimi che contengono, sono costituiti o sono prodotti a partire da OGM autorizzati presenti in una proporzione non superiore allo 0,9% per ingrediente, purché tale presenza sia accidentale o tecnicamente inevitabile – gli operatori devono quindi dimostrare alle autorità competenti di avere preso tutte le misure appropriate per evitarne la presenza.Per quanto riguarda i mangimi biologici è fatto divieto di impiego di OGM e/o prodotti derivati da OGM per la loro produzione ma è comunque valida la soglia di tolleranza dello 0,9% purché tale presenza sia accidentale o tecnicamente inevitabile
- Etichettatura mangimi– Il regolamento prevede che l’etichetta sia chiaramente visibile, leggibile e indelebile, apposta su un documento di accompagnamento oppure sulla confezione o sul contenitore;- per gli OGM destinati all’alimentazione animale e per i mangimi che contengono o sono costituiti da OGM la denominazione “(nome dell’organismo) geneticamente modificato” appare tra parentesi immediatamente dopo la denominazione specifica del mangime in questione es. Mangime semplice [mais geneticamente modificato]In alternativa tale denominazione può apparire in una nota in calce all’elenco dei mangimi es. materia prima per mangimi (mais geneticamente modificato). – per i mangimi prodotti a partire da OGM la denominazione “prodotto da (nome dell’organismo) geneticamente modificato” appare tra parentesi immediatamente dopo la denominazione specifica del mangime. es. Mangime semplice [Prodotto da mais geneticamente modificato]In alternativa tale denominazione può apparire in una nota in calce all’elenco dei mangimi.
Regolamento (CE) n. 1830/2003 del Parlamento europeo e del Consiglio, del 22 settembre 2003, concernente la tracciabilità e l’etichettatura di organismi geneticamente modificati e la tracciabilità di alimenti e mangimi ottenuti da organismi geneticamente modificati, nonché recante modifica della direttiva 2001/18/CE
Il Reg. (CE) n. 1830/2003 (in applicazione dal 18 aprile 2004) istituisce un quadro normativo per la tracciabilità dei prodotti contenenti OGM o da essi costituiti e degli alimenti e mangimi ottenuti da OGM, allo scopo di facilitare il controllo e la verifica dell’etichettatura, il monitoraggio degli effetti sulla salute e sull’ambiente nonché delle misure adeguate di gestione dei rischi, e se necessario il ritiro dei prodotti.
- Tracciabilità:
- – la tracciabilità e l’etichettatura degli OGM autorizzati deve essere garantita in tutte le fasi della loro immissione in commercio;
- – la tracciabilità degli OGM facilita il ritiro di prodotti dal mercato qualora si verifichino imprevisti effetti nocivi per la salute umana o degli animali o per l’ambiente. La tracciabilità agevola l’attuazione di misure di gestione del rischio, conformemente al principio di precauzione;
- – la tracciabilità favorisce il controllo e verifica dell’etichettatura;
- – la tracciabilità facilita, qualora necessario, il monitoraggio dei potenziali effetti sulla salute e sull’ambiente
- – la trasmissione e la conservazione dell’informazione dei prodotti contenenti o costituiti da OGM, nonché i codici esclusivi assegnati a detti OGM sono fondamentali ai fini della tracciabilità e dell’etichettatura degli OGM stessi.
Disposizioni per la tracciabilità ed etichettatura dei prodotti contenenti OGM o da essi costituiti
- – nella prima fase dell’immissione in commercio di un prodotto contenente OGM o da essi costituito gli operatori devono trasmettere per iscritto all’operatore che riceve il prodotto le seguenti informazioni:
- – l’indicazione che il prodotto contiene OGM o è da essi costituito;
- – indicazione degli identificatori unici assegnati agli OGM
In tutte le fasi successive all’immissione in commercio dei prodotti gli operatori devono assicurare la trasmissione per iscritto di tutte le informazioni necessarie lungo tutta la filiera. Le informazioni devono essere conservate per 5 anni dopo ogni transazione e tali informazioni devono essere disponibili per verifica da parte delle autorità competenti.
La tracciabilità rende obbligatorio per tutti gli operatori del settore, e cioè gli operatori che immettono un prodotto sul mercato o ricevono un prodotto che è stato immesso sul mercato all’interno della UE di potere identificare il fornitore e gli stabilimenti ai quali i prodotti sono stati inviati.
-
- Etichettatura:
Per i prodotti contenenti OGM o da essi costituiti gli operatori provvedono:
-
- – prodotti preconfezionati contenenti OGM o da essi costituiti: apporre sull’etichetta la dicitura “questo prodotto contiene organismi geneticamente modificati” o “questo prodotto contiene (nome dell’organismo/i) geneticamente modificato/i”.
- – prodotti non preconfezionati offerti al consumatore finale: la dicitura “questo prodotto contiene organismi geneticamente modificati” o “questo prodotto contiene (nome dell’organismo/i) geneticamente modificato/i”.
Quanto sopra indicato deve in ogni caso tenere conto di altri requisiti specifici previsti dalla normativa comunitaria compreso quanto specificato nel Reg. (CE) n. 1829/2003.
Disposizioni per la tracciabilità per i prodotti per mangimi ottenuti da OGM gli operatori che immettono in commercio prodotti ottenuti da OGM devono trasmettere per iscritto all’operatore che riceve il prodotto le seguenti informazioni:
- – un indicazione di ciascuna delle materie prime o degli additivi del mangime ottenuti da OGM
Le disposizioni in materia di tracciabilità ed etichettatura non si applicano alle tracce di OGM presenti in prodotti in proporzione non superiore allo 0,9% purché tali tracce di OGM siano accidentali o tecnicamente evitabili.
Regolamento (CE) n. 65/2004 della Commissione, del 14 gennaio 2004, che stabilisce un sistema per la determinazione e l’assegnazione di identificatori unici per gli organismi geneticamente modificati
- ogni operatore che immette in commercio prodotti contenenti OGM o costituiti da OGM è tenuto a includere, tra le informazioni, l’identificatore unico assegnato ad ogni OGM per indicarne la presenza e contraddistinguere lo specifico evento di trasformazione oggetto dell’autorizzazione all’immissione in commercio di tale OGM;
- le domande di immissione in commercio di OGM devono contenere un identificatore unico per ciascun OGM. I richiedenti generano l‘identificatore unico secondo i formati dell’allegato al regolamento.
- qualora sia concessa l’autorizzazione all’immissione in commercio di un OGM, l’autorizzazione deve specificare l’identificatore unico assegnato a tale OGM; Gli identificatori unici sono iscritti nei registri della Commissione.
Formato degli identificatori unici:
- Formato generale: costituito da 3 componenti che contengono un determinato numero di caratteri alfanumerici corrispondenti:
- Prima componente: richiedente/titolare autorizzazione – i primi 2 o 3 caratteri indicano il richiedente/titolare dell’autorizzazione seguiti da un trattino;
- Seconda componente: evento di trasformazione – il secondo gruppo di 5 o 6 caratteri rappresenta lo specifico evento/eventi di trasformazione, oggetto di autorizzazione;
- Terza componente: carattere ai fini di controllo ed è destinato a ridurre gli errori garantendo l’integrità del codice alfanumerico introdotto dagli utenti della banca dati. E’ composto da un unico carattere numerico ed è calcolato sommando i valori numerici di ciascuno dei caratteri dell’identificatore unico.
L’identificatore è composto da 9 caratteri alfanumerici: Es. CED-AB891-6 oppure CE-ABC891-6
- Regolamento (CE) n. 834/2007 del Consiglio, del 28 giugno 2007 , relativo alla produzione biologica e all’etichettatura dei prodotti biologici e che abroga il regolamento (CEE) n. 2092/91
- Considerato che:
- Gli organismi geneticamente modificati (OGM) e i prodotti derivati od ottenuti da OGM sono incompatibili con il concetto di produzione biologica e con la percezione che i consumatori hanno dei prodotti biologici. Essi non dovrebbero quindi essere utilizzati nell’agricoltura biologica nella trasformazione di prodotti biologici;
- L’obiettivo perseguito è quello di limitare per quanto possibile la presenza di OGM nei prodotti biologici. Le soglie di etichettatura esistenti rappresentano massimali legati esclusivamente alla presenza accidentale e tecnicamente inevitabile di OGM;
- È vietato l’uso di OGM nella produzione biologica. A fini di chiarezza e di coerenza, occorre precludere la possibilità di etichettare come biologico un prodotto che deve essere etichettato come contenente OGM, costituito da OGM o derivato da OGM;
- la progettazione e la gestione appropriate dei processi biologici fondate su sistemi ecologici che impiegano risorse naturali interne ai sistemi stessi con metodi che escludono l’uso di OGM e dei prodotti derivati o ottenuti da OGM ad eccezione dei medicinali veterinari.
Stabilisce che:
- Gli OGM e i prodotti derivati o ottenuti da OGM non vanno usati come alimenti, mangimi, ausiliari di fabbricazione, prodotti fitosanitari, concimi, ammendanti, sementi, materiale di moltiplicazione vegetativa, microrganismi e animali in produzione biologica.
- Ai fini del divieto di cui al paragrafo 1 riguardante gli OGM o prodotti derivati da OGM per alimenti e mangimi, gli operatori possono fare affidamento sull’etichetta o qualsiasi altro documento che accompagna un prodotto e che sia apposto o fornito ai sensi della direttiva 2001/18/CE, del regolamento (CE) n. 1829/2003 del Parlamento europeo e del Consiglio, del 22 settembre 2003, relativo agli alimenti e ai mangimi geneticamente modificati, o del regolamento (CE) n. 1830/2003.
- Se gli alimenti o i mangimi acquistati non sono etichettati né accompagnati da un documento, ai sensi dei suddetti regolamenti, gli operatori possono presupporre che nella produzione degli stessi non si è fatto uso di OGM o di prodotti derivati da OGM, a meno che non dispongano di altre informazioni secondo le quali l’etichettatura dei prodotti in questione non è in conformità con i suddetti regolamenti.
- Ai fini del divieto di cui al paragrafo 1 riguardante i prodotti diversi da alimenti o mangimi o prodotti ottenuti da OGM, gli operatori che usano tali prodotti non biologici acquistati da terzi chiedono al venditore di confermare che gli stessi non sono derivati o ottenuti da OGM.
NORMATIVA DI RIFERIMENTO RELATIVA AL CAMPIONAMENTO NEL CONTROLLO UFFICIALE
Regolamento (UE) n. 691/2013 della Commissione, del 19 luglio 2013 , che modifica il regolamento (CE) n. 152/2009 per quanto riguarda i metodi di campionamento e di analisi.
La metodologia di campionamento deve fare riferimento al Reg. (CE) 152/2009 che fissa i metodi di campionamento e d’analisi per i controlli ufficiali degli alimenti per gli animali cosi come modificato da Reg. (UE) 691/2013 “metodi di campionamento ed analisi ” che si applica anche agli OGM classificandoli come analiti distribuiti in modo non uniforme e quindi il campionamento segue delle regole particolari.
Gli analiti distribuiti in modo non uniforme nelle materie prime risultano essere distribuiti in modo uniforme nei mangimi composti a seguito dell’attività di miscelazione. Quindi, per le materie prime per mangimi il campionamento deve essere effettuato secondo quanto indicato al punto 5.2 dell’allegato I del Reg. (UE) n. 691/2013, mentre per i mangimi composti possono essere usati i metodi previsti per analiti distribuiti in modo uniforme, come indicato al punto 5.1 del Regolamento. Questa distinzione è riportata anche nel Piano Nazionale di Controllo Ufficiale sull’Alimentazione degli Animali (triennio 2018-2020) e le procedure da seguire sono dettagliate nell’allegato 8 sul campionamento, tabella 2 per analiti ripartiti in modo uniforme, tipologia di distribuzione A e tabella 3 per analiti ripartiti in modo non uniforme, tipologia di distribuzione B. Nelle seguenti tabelle dell’allegato 8, sono riportati i requisiti quantitativi per effettuare il campionamento stabiliti in base alle dimensione e alle caratteristiche della partita da campionare.
PER MANGIMI CON ANALITA DISTRIBUITO IN MODO NON UNIFORME (MANGIMI SEMPLICI IN GRANELLA E INSILATI) – tabella 2
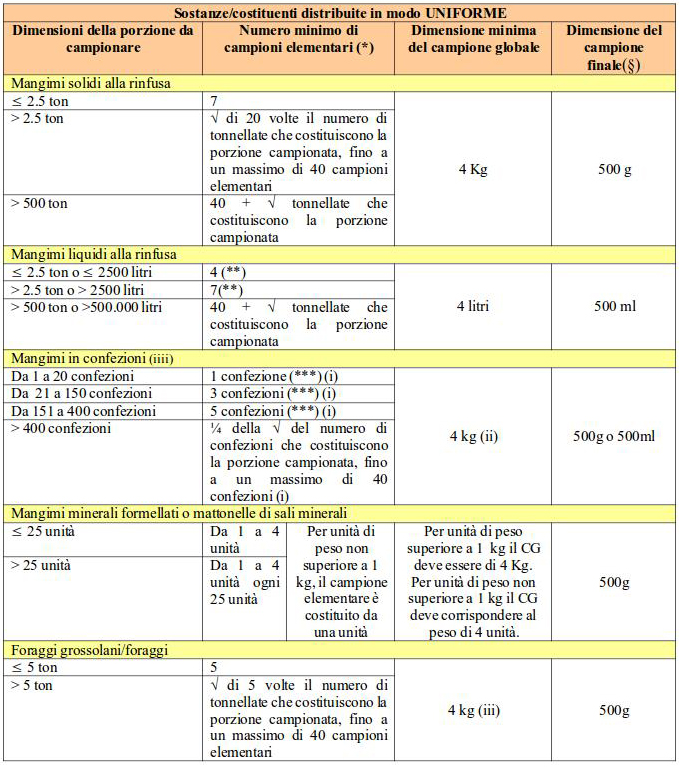
PER MANGIMI CON ANALITA DISTRIBUITO IN MODO UNIFORME (MANGIMI COMPLETI E COMPLEMENTARI) – tabella 3
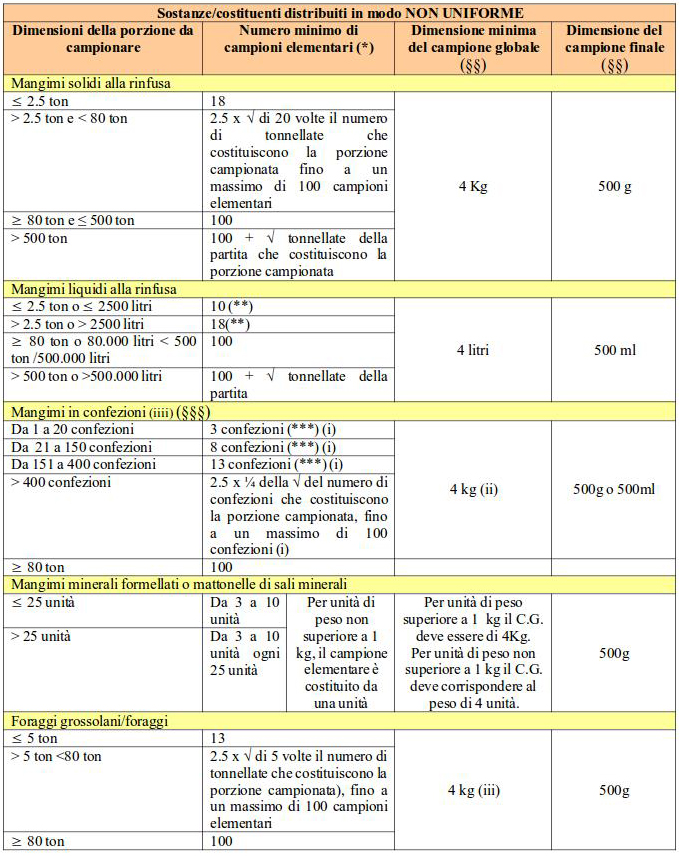
(*) Se il risultato del calcolo è un numero decimale, si arrotonda al numero intero superiore.
(**) Nel caso in cui non sia possibile rendere omogeneo il liquido, il numero di campioni elementari deve essere aumentato.
(***) Per le confezioni di contenuto non superiore a 1 kg o a un litro, il campione elementare è costituto dal contenuto di un confezione originaria.
(i) Qualora l’apertura di confezione possa alterare i risultati dell’analisi (per esempio nel caso di mangimi umidi deperibili), il campione elementare è costituito da una confezione non aperta.
(ii) Nel caso degli alimenti confezionati, è possibile che le dimensioni delle singole unità non consentano di prelevare 4 kg per il campione globale.
(iii) Qualora si tratti di foraggio grossolano o foraggio a basso peso specifico (ad esempio fieno o paglia), il campione globale deve essere di almeno 1 kg.
(iiii) Le confezioni (sacchi, fusti, barattoli) di grandi dimensioni con contenuti superiori o uguali a 500 litri o kg, devono essere campionati come prescritto per i mangimi solidi o liquidi alla rinfusa.
(§) per la determinazione dei radionuclidi il CF deve essere sempre di 1Kg.
(§§) Per granelle prelevate per la ricerca di OGM nel contesto del Regolamento (UE) 619/2011 i quantitativi minimi di riferimento sono specificati al capitolo 9.
(§§§) Per la ricerca di Salmonella spp. in snack dog-chews, in confezioni molto piccole (o singole), è previsto di campionare un numero di confezioni appartenenti al medesimo lotto di produzione tale da consentire la formazione di un CG (composto da minimo 4 confezioni) dal quale sia possibile ottenere CF ciascuno di un peso minimo di 100 grammi.
In generale il numero minimo di CE per la tipologia B (distribuzione non uniforme) corrisponde al numero di CE che deve essere preso per la tipologia A (uniforme) moltiplicato per un fattore pari a 2,5.
Ad esempio per un lotto di materie prime in granella (tipologia di distribuzione B) delle dimensione di 50 tonnellate si procede come riportato nella tabella 1 per mangimi solidi alla rinfusa di dimensioni comprese tra 2.5 ton e < 80 ton.
Il numero dei CE è dato da : 2.5 x √ di 20 volte il numero di tonnellate della partita da campionare quindi ; 2,5 x √20 x50 = √ 1000 x 2,5 = 32 x 2,5 = 80 CE da 100g (CG 8 kg). Ad esempio per una partita di 75 t di mangimi in confezioni formata da 300 unità di mangime semplice (tipologia di distribuzione B ) in sacchi da 25 kg si procede come indicato nella tabella 1 mangimi in confezioni nel range 151 – 400 confezioni.
Il numero dei CE è uguale a 13 (2,5 x 5) da 308g per ottenere un CG da 4 kg.
Modalità di campionamento
I campioni elementari (CE) vanno prelevati a caso, tenendo in considerazione la rappresentatività dell’insieme della porzione da campionare, ogni CE deve avere approssimativamente lo stesso peso che non deve essere inferiore a 100 grammi.
Il tipo di campionamento, in base alla tipologia di lotto da campionare ed al luogo di prelievo, può essere statico o dinamico.
Nel campionamento statico i prelievi vengono effettuati in punti specifici ripartiti sulla massa non in movimento come riportato nella Norma ISO 24333:2009 (prelievo in punti diversi di una massa stoccata), operando sulle superfici libere della massa stessa. Può essere eseguito mediante attrezzature automatiche o manualmente con pale a bordi rialzati o sonde. Il margine di errore per questa modalità, di per sé più alto rispetto al prelievo dinamico, , decresce progressivamente al diminuire della massa campionata (vagone > silos > sacchi> piccole confezioni).
Nel campionamento dinamico i prelievi vengono effettuati in tempi diversi da una massa in movimento (per merci alla rinfusa) come riportato nella Norma ISO 24333:2009. Il prelievo può essere eseguito in modalità manuale o in automatico (campionatori), prelevando i CE da nastri trasportatori o da masse in flusso (es. durante il carico o lo scarico). La frequenza di prelievo dei campioni elementari (intesa come intervallo di tempo) è in funzione della velocità di flusso, delle dimensioni della matrice e del campione globale da prelevare.Gli operatori andrebbero incoraggiati ad installare attrezzature che consentano di effettuare il campionamento automatico per facilitare e ottimizzare le operazioni di campionamento. Il campione globale è ottenuto dall’insieme di tutti i CE prelevati dalla partita e deve essere omogeneizzato con l’utilizzo di un apposito contenitore, mediante opportuna (per tempo e portata) e accurata mescolatura. Se necessario il CG omogeneizzato (CGO) può essere “ridotto” ad un peso di 2 Kg. Dal CGO o dal campione ridotto si preparano i campioni finali (CF) che devono essere almeno 4..
Per le materie prime in granella, al fine di garantire una distribuzione uniforme dell’analita nei CF, i C.F. sono ottenuti dalla macinazione del CGO o del campione ridotto, con apposita apparecchiatura o da banco o industriale. Tale operazione deve essere effettuate da personale adeguatamente formato, con attrezzature idonee, presso locali con adeguati requisiti strutturali appositamente individuati dalle Autorità regionali (generalmente presso gli IZZSS). Per gli OGM, la macinazione può essere effettuata esclusivamente a secco senza utilizzare la tecnica di slurry. La fase di macinazione consente di ottenere una migliore attendibilità dei risultati di laboratorio in quanto aumenta la rappresentatività ed omogeneità dei CF tra di loro e quindi anche la, riproducibilità delle analisi effettuate da laboratori di prima e seconda istanza o I CF devono essere consegnati al laboratorio nel più breve tempo possibile e comunque non oltre le 48 ore.
Regolamento (UE) n. 619/2011 della Commissione, del 24 giugno 2011 , che fissa i metodi di campionamento e di analisi per i controlli ufficiali degli alimenti per animali riguardo alla presenza di materiale geneticamente modificato per il quale sia in corso una procedura di autorizzazione o la cui autorizzazione sia scaduta.
Il presente Regolamento si applica ai controlli ufficiali sui mangimi al fine di verificare la presenza di OGM in corso di autorizzazione (quindi non ancora autorizzati nell’Unione Europea) o la cui autorizzazione sia scaduta. Il materiale geneticamente modificato (GM) in questione deve essere commercializzato in un paese terzo e deve essere stata presentata una domanda di autorizzazione valida ai sensi del Reg(CE) 1829/2003; non devono essere stati evidenziati,da parte dell’Autorità Europea per la Sicurezza Alimentare (EFSA), effetti nocivi sulla salute e sull’ambiente del materiale GM e devono essere noti e fruibili, ai laboratori che effettuano le analisi per il controllo ufficiale, il Materiale di Riferimento Certificato e il metodo quantitativo già precedentemente convalidato e pubblicato dal Laboratorio Europeo di Riferimento.
Il presente regolamento si applica anche al materiale GM la cui autorizzazione sia scaduta.
Per la verifica della presenza di materiale GM il campione globale/ridotto deve permettere di ottenere campioni finali di almeno 10 000 semi/sementi e pertanto la dimensione del campione globale non deve essere inferiore al peso corrispondente a 40 000 semi/sementi.
Per campioni globali contenenti almeno 40000 semi, per il mais il campione globale deve essere di almeno 12 kg, per la soia 8 kg e per altri semi e grani come orzo, avena, miglio, riso, segale, frumento e colza almeno 4 kg. Nella tabella 3 si riporta il riepilogo dei campionamenti di materie prime in granella per la ricerca di OGM non autorizzati che hanno una distribuzione non uniforme nei mangimi..
| Specie Vegetale | Campione finale (g)(corrisp. a 10 000 semi/sementi) | Campione globale minimo in kg |
|---|---|---|
| Orzo, miglio, avena, riso, segale, frumento | 400 | 4 |
| Granoturco | 3000 | 12 |
| Soia | 2000 | 8 |
| Semi di colza | 40 | 4 |
Ciascun campione globale deve essere successivamente omogeneizzato mediante mescolatura (strumentazione pulita) ed inviato al laboratorio di analisi dove avverrà la fase relativa alla formazione dei campioni finali seguendo le stesse procedure sopra riportate.
I laboratori ufficiali devono soddisfare i requisiti della norma ISO 17025 e usare metodi d’analisi quantitativi convalidati dal laboratorio di riferimento dell’Unione europea in collaborazione con la rete europea dei laboratori OGM (European Network of GMO Laboratories). Considerando l’intero metodo analitico a partire dal trattamento del campione di laboratorio del mangime, essi devono garantire di essere in grado di effettuare le analisi con adeguata precisione a livello dello 0,1 % riferito alla frazione di massa del materiale GM nel mangime (deviazione standard relativa di ripetibilità pari o inferiore al 25 %). Tale limite dello 0,1% è definito come limite minimo di rendimento richiesto (LMRR). La decisione sulla non conformità di un mangime può essere presa solo quando il materiale GM, che rientri nel campo di applicazione di questo regolamento, è presente a livelli pari o superiori all’LMRR, tenuto conto dell’incertezza di misurazione.
FLUSSO ANALITICO PER LA RICERCA DI OGM
(il presente allegato si riferisce esclusivamente agli OGM autorizzati nell’Unione Europea)
Durante il processo di autorizzazione di un nuovo evento GM il richiedente è tenuto a fornire il metodo analitico per il rilevamento e la quantificazione dell’evento di trasformazione sottoposto ad autorizzazione, insieme a materiali di riferimento e controlli. Il metodo di rilevazione (qPCR) viene poi validato dal laboratorio europeo di riferimento (EURL – European Union Reference Laboratory – http://gmo-crl.jrc.ec.europa.eu/ ), assistito dalla rete europea di laboratori OGM (ENGL – European Network of GMO Laboratories). I materiali di riferimento e i metodi validati sono resi pubblici e sono disponibili per i laboratori che svolgono analisi OGM.
I metodi quantitativi adottati nell’UE consistono di due sistemi di amplificazione in PCR real time, uno specifico per l’evento geneticamente modificato, l’altro specifico per la specie di appartenenza dell’evento geneticamente modificato (ad es. soia, mais, cotone etc). Dalla combinazione dei risultati ottenuti dalle due reazioni, l’analista è in grado di effettuare una quantificazione relativa dell’evento geneticamente modificato in oggetto rispetto alla specie di appartenenza. In questo modo è possibile confrontare la percentuale riscontrata nel campione con il limite legale dello 0,9%, oltre il quale è obbligatorio specificare in etichetta la presenza di tale ingrediente geneticamente modificato nel prodotto alimentare.
Nella definizione del flusso analitico, prima di arrivare all’eventuale quantificazione dell’evento, è tuttavia opportuno prevedere dei passaggi preliminari che consentono di ottimizzare i costi. Il flusso inizia con la verifica della presenza della specie vegetale che costituisce il mangime (soia, mais, cotone etc), mediante la ricerca del relativo sistema di riferimento specie specifico (sistema endogeno). Una volta riscontrata la presenza della specie vegetale/ingrediente nel campione si procede con ulteriori indagini a diverso grado di specificità, che conducono all’identificazione di eventuali OGM:
- Identificazione di elementi genetici (codificanti o regolativi) presenti in diversi OGM, (Screening): sono generalmente utilizzati per effettuare lo screening per la presenza/assenza di OGM nel campione, in quanto sono spesso inseriti in molte piante transgeniche attualmente commercializzate. Quelli maggiormente utilizzati sono ad esempio il promotore 35S, il terminatore Nos, il gene cp4-epsps, il gene nptII, il gene pat, il gene bar ed altri ancora. Il rilevamento di queste sequenze non è comunque sufficiente a dimostrare la presenza di un OGM e a questo livello di specificità non è possibile identificare l’OGM responsabile di eventuali positività. Per questo motivo è sempre necessario procedere con test a specificità maggiore.
- Identificazione di singoli eventi GM (Fig. 1): ciascun costrutto genico si inserisce in un punto del DNA della pianta che è unico e che caratterizza l’evento GM. I metodi evento specifici hanno come bersaglio la regione di giunzione unica tra il DNA transgenico e il DNA della pianta. Tale livello di specificità è quello richiesto dalla normativa europea.
- Quantificazione dei singoli eventi GM precedentemente identificati
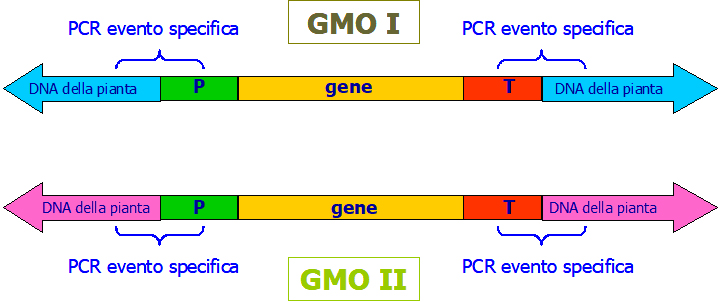
Figura 1: mostra due eventi GMO diversi (GMO I e II) che presentano lo stesso costrutto (P: promotore, sequenza codificante e T: terminatore). Per esempio il mais Bt10 e il mais Bt11 sono 2 eventi con lo stesso costrutto, ma mentre il secondo risulta autorizzato, per il primo non ha mai stata inoltrata richiesta di autorizzazione.
Nella figura 2 è schematizzato il flusso analitico sopra descritto, normalmente utilizzato per i campioni del controllo ufficiale, mentre nella figura 3 vengono fornite indicazioni riguardo l’autocontrollo.
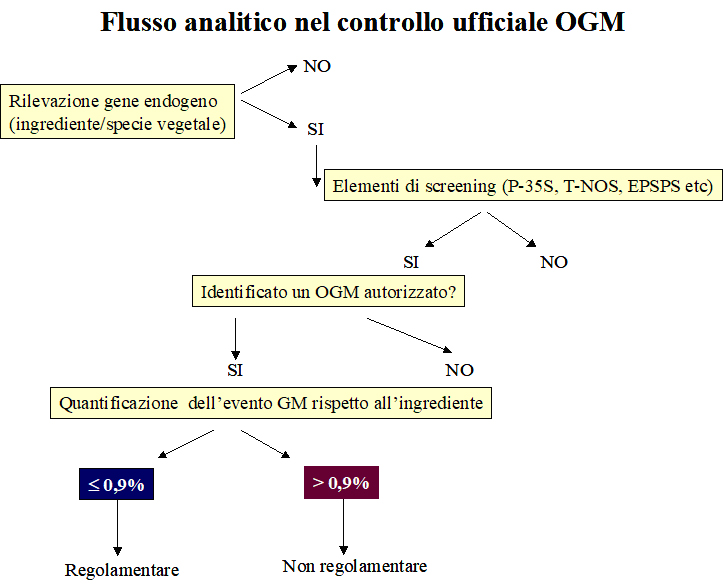
Figura 2: rappresentazione schematica del flusso analitico utilizzato per l’identificazione e quantificazione di OGM autorizzati nell’Unione Europea.
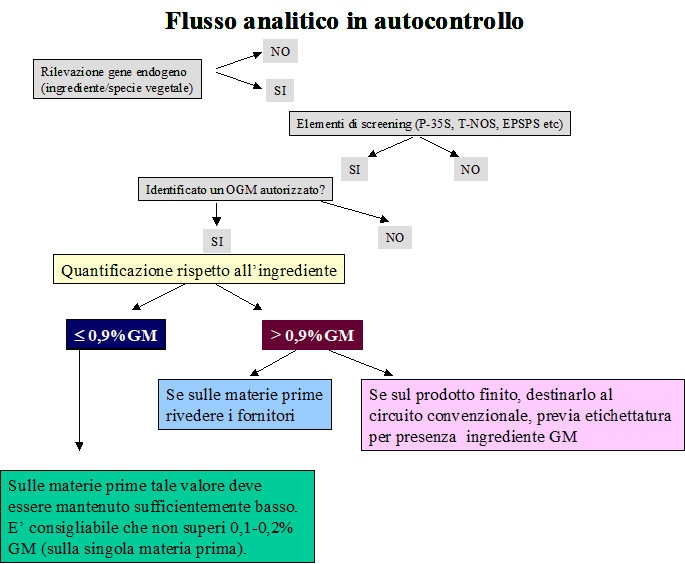
Figura 3: rappresentazione schematica del possibile flusso analitico in autocontrollo con particolare riferimento al controllo delle materie prime utilizzate.
Linee guida per la gestione delle produzioni mangimistiche nella filiera non-ogm – (Versione PDF)
